This is a SEO version of Microsoft Word - PHYSIK.doc. Click here to view full version
« Previous Page Table of Contents Next Page »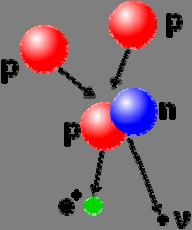

Illustration einer Kernfusion, bei dem zwei Protonen zu einem Deuteriumkern aus einem Proton und einem Neutron reagieren. Ein Positron (e + ) – das Antiteilchen des Elektrons – und ein Elektron-Neutrino entstehen bei der Reaktion.
Größere Atomkerne können aus kleineren Kernen gebildet werden. Dieser Vorgang wird Kernfusion genannt. Es ist so, dass sich Atomkerne für die Fusion sich sehr nah kommen müssen. Diesem Annähern steht die elektrostatische Abstoßung der positiv geladenen Protonen, der sogenannte Coulombwall entgegen. Aus diesem Grund ist eine Kernfusion nur unter sehr hohen Temperaturen von mehreren Millionen Grad und hohen Drücken, wie sie im Inneren von Sternen herrschen, möglich. Bei der Kernfusion werden durch Umwandlung von Masse in Energie gemäß der Äquivalenz von Masse und Energie, E = mc 2 große Mengen Energie frei. Diese Energie äußert sich im Massendefekt und entspricht der Bindungsenergie des Atomkerns. Die Kernfusion ist bei Elementen bis zum Eisen eine exotherme Reaktion, so dass sie selbsterhaltend ist und in Sternen kontinuierlich weiterläuft. Bei Atomkernen die größer sind als der des Eisens, nimmt die Bindungsenergie ab und die Fusion schwererer Atomkerne ist daher endotherm. Sie ist damit kein selbsterhaltender Prozess, was dazu führt, dass die Kernfusion in Sternen zum Erliegen kommt, wenn die leichten Atomkerne aufgebraucht sind.
Atomhülle
Die Atomhülle besteht aus den negativ geladenen Elektronen und umgibt den Kern. Sie ist etwa 10.000-mal größer als dieser und bestimmt damit die Größe des Atoms. Gleichzeitig sind die Elektronen mit einer Masse von 9,11 × 10 −31 kg so leicht, dass die Elektronenhülle praktisch nichts zur Masse des Atoms beiträgt. Sie sind zudem so klein, dass mit derzeitigen Messmethoden keine Ausdehnung festgestellt werden kann.
Aufbau
Elektronen werden, wie alle Teilchen, in der Quantenmechanik durch eine Wellenfunktion beschrieben, die die Wahrscheinlichkeit angibt, mit der das Elektron in einem bestimmten Gebiet zu finden ist. Diese Wellenfunktion wird mit der Schrödingergleichung beschrieben, die die potentielle und kinetische Energie des Elektrons im Potential des Kerns beschreibt. Sie ist exakt nur für das Wasserstoffatom und wasserstoffähnliche Atome mit nur einem Elektron lösbar. Für kompliziertere Systeme mit mehreren Elektronen wird das Orbitalmodell als gute Nährung verwendet. Bei diesen gilt das Pauli-Prinzip, nachdem sich jedes Elektron in mindestens einem Zustand, repräsentiert durch unterschiedliche Quantenzahlen, unterscheiden muss. Dies führt dazu, dass jedes Orbital mit lediglich zwei Elektronen mit entgegengesetztem Spin, einer Art Eigendrehung des Elektrons, besetzbar ist, siehe Elektronenkonfiguration.
Eigenschaften
Die Atomhülle bestimmt maßgeblich viele Eigenschaften des gesamten Atoms. Je mehr Elektronen in der Hülle enthalten sind, desto größer ist ihre Ausdehnung. Allerdings ist diese diffus und besitzt keine exakt definierbare äußere Grenze. Daher wird ihre Größe üblicherweise durch den Abstand der Atomkerne zweier chemisch gebundener Atome angegeben. Neben der Anzahl der Elektronen und der Stärke ihrer Bindung an den Kern spielt auch die Umgebung, etwa die Anzahl benachbarter Atome eine Rolle für die Größe eines Atoms. Im Periodensystem gilt
This is a SEO version of Microsoft Word - PHYSIK.doc. Click here to view full version
« Previous Page Table of Contents Next Page »