This is a SEO version of Microsoft Word - PHYSIK.doc. Click here to view full version
« Previous Page Table of Contents Next Page »was etwa „das Unzerschneidbare“ bedeutet, also ein nicht weiter zerteilbares Objekt bezeichnet. Obwohl die indischen und griechischen Atomvorstellungen rein philosophischer Natur waren, hat die moderne Chemie die Bezeichnung von Demokrit beibehalten.
Bis zur Entwicklung der Chemie als Wissenschaft brachte das Atomkonzept keine neuen Erklärungen. 1661 publizierte der Naturphilosoph Robert Boyle sein Werk The Sceptical Chymist , in dem er argumentierte, die Materie sei aus diversen Kombinationen verschiedener „corpuscules“ aufgebaut und nicht aus den vier Elementen Wasser, Erde Feuer und Luft. [ 1789 prägte Antoine Lavoisier den Begriff Element für Grundstoffe, die mit chemischen Methoden nicht weiter zerlegt werden können.
Naturwissenschaftliche Forschung
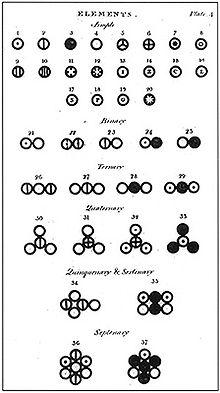
Verschiedene Atome und Moleküle, wie sie in
A New System of Chemical Philosophy (1808) von John Dalton abgebildet sind.
1803 benutzte der englische Lehrer und Naturphilosoph John Dalton das Atomkonzept, um zu erklären, wieso Elemente immer in Verhältnissen kleiner ganzer Zahlen miteinander reagieren – Gesetz der multiplen Proportionen – und weshalb bestimmte Gase sich besser in Wasser lösen als andere. Er nahm an, dass jedes Element aus einer einzigartigen Sorte von Atomen besteht und dass diese Atome sich miteinander verbinden und dadurch chemische Verbindungen bilden.
1827 erhielt die Atomtheorie durch die Beobachtungen des Botanikers Robert Brown zusätzliche Unterstützung. Er stellte bei Untersuchungen mit dem Mikroskop fest, dass Pollen und Staubkörner in Wasser sich ungeordnet hin und her bewegten – ein Phänomen, dass als Brownsche Bewegung bekannt wurde. Diese Beobachtung wurde durch eine mathematische Untersuchung Albert Einsteins von 1905 als Effekt von Stößen mit Wassermolekülen, die sich thermisch bewegen, erklärt. Der französische Physiker Jean Perrin benutzte Einsteins Arbeit, um experimentell Masse und Größe von Atomen zu bestimmen, und bestätigte damit Daltons Atomtheorie.
Joseph John Thomson entdeckte 1897 bei seiner Arbeit mit Kathodenstrahlen das Elektron und stellte fest, dass es ein Bestandteil von Atomen ist, womit er das Konzept des Atoms als unzerteilbarer Einheit zerstörte. [12] Thomson glaubte, dass die Elektronen im Atom verteilt seien und ihre Ladung durch ein gleichmäßiges, positiv geladenes Medium kompensiert würde (Thomsonsches Atommodell).
Eine Forschungsgruppe um Ernest Rutherford beschoss 1909 eine Goldfolie mit (positiv geladenen) Heliumatomkernen (Alphastrahlung) und stellte fest, dass ein kleiner Anteil der Teilchen um sehr viel größere Winkel abgelenkt wurden, als Thomsons Modell es vorhersagte. Rutherford schloss aus diesem Experiment, dass die positive Ladung eines Atoms und der Großteil
This is a SEO version of Microsoft Word - PHYSIK.doc. Click here to view full version
« Previous Page Table of Contents Next Page »