This is a SEO version of Microsoft Word - PHYSIK.doc. Click here to view full version
« Previous Page Table of Contents Next Page »seiner Masse in einem Atomkern in der Mitte des Atoms konzentriert sei und die Elektronen um diesen Kern kreisten wie die Planeten um die Sonne (Rutherfordsches Atommodell). Die positiv geladenen Teilchen, die sehr nah an diesen Kern kamen, würden sehr viel stärker abgelenkt, als andere.
Bei Experimenten mit den Produkten radioaktiver Zerfälle stellte der Radiochemiker Frederick Soddy 1913 fest, dass es anscheinend mehr als eine Atomart für jedes Element gab. Der Begriff Isotop für verschiedene Atome desselben Elements wurde von Margaret Todd geprägt. J. J. Thomson entwickelte bei seiner Arbeit über ionisierte Gase ein Verfahren zur Trennung verschieden schwerer Atome, was zur Entdeckung stabiler Isotope führte.
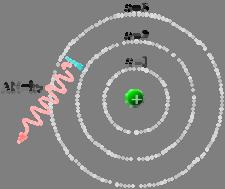

Illustration des bohrschen Modells des Wasserstoffatoms mit einem Elektron, das zwischen festen Umlaufbahnen (Orbits) springt und dabei ein Photon mit einer bestimmten Frequenz abstrahlt.
1913 überarbeitete Niels Bohr Rutherfords Atommodell und nahm an, dass die Elektronen sich nur auf bestimmten quantisierten Umlaufbahnen (Schalen) aufhalten und zwischen diesen „springe“, sich jedoch nicht in Zwischenzuständen aufhalten könnten. Ein Elektron muss eine bestimmte Menge an Energie aufnehmen oder abgeben, um zwischen diesen festen Schalen zu wechseln. Wenn das Licht, das von einem erhitzten Material abgestrahlt wird, durch ein Prisma geleitet wird, erzeugt es ein farbiges
Emissionsspektrum. Die Existenz fester Spektrallinien in diesen Spektren wurde erfolgreich durch die Übergänge des Elektrons zwischen den Schalen im Atome erklärt.
Chemische Bindungen wurden 1916 von Gilbert Newton Lewis im Rahmen des bohrschen Atommodells durch Wechselwirkung der Elektronen der Bestandteile erklärt. Um zu erklären, dass sich die chemischen Eigenschaften der Elemente grob periodisch mit der Ordnungszahl verhalten, schlug Irving Langmuir 1919 vor, dass Elektronen in einem Atom verbunden oder verklumpt seien. Elektronengruppen besetzten nach dieser Vorstellung bestimmte Elektronenschalen um den Kern.
Der Stern-Gerlach-Versuch von 1922 erbrachte neue Erkenntnisse über die quantenmechanischen Eigenschaften von Atomen. Ein Strahl aus Silberatomen, der durch ein speziell geformtes Magnetfeld geleitet wird, spaltet sich abhängig von der Richtung des Drehimpulses des äußersten Elektrons des Atoms auf. Es wurde erwartet, dass diese Richtung zufällig ist und der Strahlquerschnitt eine Linie beschreiben würde. Stattdessen wurde der Strahl in zwei Teile aufgespalten, was darauf hindeutete, dass nur zwei Ausrichtungen des Drehimpulses oder Spins vorkommen.
Aufbauend auf dem von Louis de Broglie 1924 postulierten Welle-Teilchen-Dualismus entwickelte Erwin Schrödinger 1926 ein Atommodell, das die Elektronen als dreidimensionale Wellen und nicht als Teilchen beschreibt. Eine Folge der Beschreibung durch Wellen ist, dass es unmöglich ist, genaue Werte sowohl für Ort als auch Impuls eines Elektrons zu erhalten. Dieser Sachverhalt wurde als Unschärferelation 1926 von Werner Heisenberg im Kontext eines verwandten Modells beschrieben. Nach der Unschärferelation können nur
Wahrscheinlichkeitsverteilungen für Wertebereiche von Ort und Impuls angegeben werden. Obwohl sich dieses Modell schwer bildlich darstellen ließ, gelang es damit sehr viel besser als mit den Vorläufermodellen, die Eigenschaften insbesondere größerer Atome als Wasserstoff, wie z. B. ihre Spektrallinien
This is a SEO version of Microsoft Word - PHYSIK.doc. Click here to view full version
« Previous Page Table of Contents Next Page »